Nội dung Bài thực hành số 4 Tính chất của oxi, lưu huỳnhcủng cố những kiến thức về tính chất hóa học của Oxi, lưu huỳnh: Tính oxihóa mạnh. Ngoài ra lưu huỳnh còn có tính khử.Chứng minh sự ảnh hưởng của nhiệt độ đến tính chất vật lí của Lưu huỳnh. Tiếp tục rèn luyện các thao tác thí nghiệm như thực hiện các phản ứng đốt cháy, tỏa nhiệt; làm thí nghiệm an toàn, chính xác; quan sát hiện tượng hóa học.
Bạn đang xem: Bài thực hành số 4 hóa học 10
1. Tóm tắt lý thuyết
1.1. Nội dung ôn tập
1.2. Một số quy tắc an toàn trong phòng thí nghiệm
2. Bài tập minh hoạ
2.1.Thí nghiệm 1: Tính oxi hóa của oxi
2.2.Thí nghiệm 2:Sự biến đổi trạng thái của Lưu huỳnh theo nhiệt độ
2.3.Thí nghiệm 3:Tính oxi hóa của Lưu huỳnh
2.4.Thí nghiệm 4: Tính khử của Lưu huỳnh
3. Luyện tập Bài 31 Hóa học 10
3.1. Trắc nghiệm
4. Hỏi đáp về Bài 31 Chương 6 Hóa học 10

1.1.1. Thí nghiệm 1: Tính oxi hóa của oxi
Phản ứng của O2 với Fe: 3Fe + 2O2
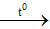
Sắt từ oxit Fe3O4 = FeO. Fe2O3
1.1.2. Thí nghiệm 2:Sự biến đổi trạng thái của Lưu huỳnh theo nhiệt độLưu huỳnh rắn màu vàng → chất lỏng màu vàng linh động → quánh nhớt màu nâu đỏ→ Lưu huỳnh màu da cam.
1.1.3. Thí nghiệm 3:Tính oxi hóa của Lưu huỳnhPhản ứng giữa Fe và S: Fe + S
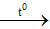
Phản ứng : S+ O2
1) Chỉ được làm thí nghiệm khi có sự hiện diện của giáo viên trong phòng thí nghiệm.
2) Đọc kỹ hướng dẫn và suy nghĩ trước khi làm thí nghiệm.
3) Luôn luôn nhận biết nơi để các trang thiết bị an toàn.
4) Phải mặc áo choàng của phòng thí nghiệm.
5) Phải mang kính bảo hộ.
6) Phải cột tóc gọn lại.
7) Làm sạch bàn thí nghiệm trước khi bắt đầu một thí nghiệm.
8) Không bao giờ được nếm các hóa chất thí nghiệm. Không ăn hoặc uống trong phòng thí nghiệm.
9) Không được nhìn xuống ống thí nghiệm.
10) Nếu làm đổ hóa chất hoặc xảy ra tại nạn, báo cho giáo viên ngay lập tức.
11) Rửa sạch da khi tiếp xúc với hóa chất.
12) Nếu hóa chất rơi vào mắt, phải đi rửa mắt ngay lập tức.
13) Bỏ chất thải thí nghiệm vào đúng nơi qui định như được hướng dẫn.
Cách tiến hành:
Gắn mẫu than gỗ vào đầu đoạn dây thép để làm mồi sao cho để đốt cháy không bị rơi.
Đốt nóng một đoạn dây thép xoắn (có gắn mẫu than ở đầu để làm mồi) trên ngọn lửa đèn cồn rồi đưa nhanh vào bình đựng khí O2.
Lưu ý: Cần làm sạch và uốn sợi dây thép thành hình xoắn lò xo để tăng diện tiếp xúc, phản ứng xảy ra nhanh hơn.Mẫu than gỗ cá tác dụng làm mồi vì khi cháy than, tạo ra nhiệt lượng đủ lớn để phản ứng giữa Fe và O2 xảy ra (có thể thay mẫu than bằng đoạn que diêm).Để an toàn cần cho vào dưới đáy bình thủy tinh một ít cát sạch để tránh vỡ lọ thủy tinh.Xem thêm: Top Máy Chụp Hình Du Lịch Dành Cho Phái Đẹp, 10 Máy Ảnh Du Lịch Tốt Nhất Giá Rẻ Đến Cao Cấp
Video 1: Phản ứng giữa đoạn dây Sắt và oxi
Hiện tượng:Mẫu than cháy hồng khi đưa vào lọ chứa Oxi, dây thép cháy trong Oxi sáng chói, nhiều hạt nhỏ sáng bắn như pháo hoa.Giải thích: Do xảy ra phản ứng: 3Fe + 2O2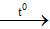
Cách tiến hành: Đun nóng Lưu huỳnh khoảng bằng 2 hạt ngô liên tục trong ống nghiệm (hoặc cốc sứ) trên ngọn lửa đèn cồn.Lưu ý:Cần hướng ống nghiệm về phía không có người và tránh hít phải hơi Lưu huỳnh độc.
Video 2: Tính chất vật lí của lưu huỳnh
Hiện tượng:Lưu huỳnh rắn màu vàng→ chất lỏng màu vàng linh động→ quánh nhớt màu nâu đỏ→ Lưu huỳnh màu da cam.Giải thích:Nhiệt độ | Trạng thái | Màu sắc | Cấu tạo phân tử |
0C | Rắn | Vàng | Vòng S8 |
1190C | Lỏng linh động | Vàng | Vòng S8 |
1870C | Lỏng quánh nhớt | Nâu đỏ | Chuỗi S8 → Sn |
4450C | Hơi | Vàng | Chuỗi Sn → Snhỏ |
14000C | Hơi | Vàng | Chuỗi S2 |
17000C | Hơi | Vàng | Nguyên tử S |
Cách tiến hành:Cho vào ống nghiệm khô một lượng hỗn hợp Fe và S khoảng bằng 2 hạt ngô.Kẹp chắt ống nghiệm trên giá thí nghiệm.Đun nóng ống nghiệm bằng đèn cồn.Lưu ý: Bột Fe phải bảo quản trong lọ kín (tốt nhất là bột sắt mới điều chế), khô.Hỗn hợp bột Fe và S được tạo theo tỷ lệ 7:4 về khối lượng và phải dùng ống nghiệm thủy tinh trung tính, khô.
Video 3: Phản ứng giữa sắt và lưu huỳnh
Hiện tượng:Phản ứng xảy ra mãnh liệt , tỏa nhiệt nhiệt, làm đỏ rực hỗn hợp.Giải thích: Phản ứng giữa Fe và S: Fe + S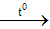
Cách tiến hành: Cho một lượng Lưu huỳnh bằng hạt ngô vào muỗng lấy hóa chất hoặc dùng đũa thủy tinh hơ nóng, nhúng đầu đũa vào bột Lưu huỳnh.Đốt cháy Lưu hùynh trên ngọn lửa đèn cồn.Mở nắp lọ thủy tinh đựng đầy khó O2 , cho nhanh chóng (hoặc đũa thủy tinh) có Lưu huỳnh đang cháy vào lọ.Lưu ý:Khí SO2 mùi hắc khó thở là khí độc nên phải cẩn thận khi làm thí nghiệm , nên sau khi đốt xong cần đậy nắp lọ ngay , tránh hít phải khí này
Video 4: Phản ứng giữa lưu huỳnh và oxi
Hiện tượng:Lưu hùynh cháy trong lọ chứa O2 mãnh liệt hơn nhiều khi cháy trong không khí.Giải thích: S+ O2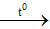
Sau bài học cần nắm:
Tính chất hóa học của Oxi, lưu huỳnhChứng minh sự ảnh hưởng của nhiệt độ đến tính chất vật lí của Lưu huỳnh.Tiếp tục rèn luyện các thao tác thí nghiệm như thực hiện các phản ứng đốt cháy, tỏa nhiệt; làm thí nghiệm an toàn, chính xác; quan sát hiện tượng hóa học.Bài kiểm tra Trắc nghiệm Hóa học 10 Bài 31 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
Câu 1:Đốt nóng thìa sắt nhỏ có chứa lưu huỳnh bột trên ngọn lửa đèn cồn, lưu huỳnh nóng chảy, sau đó cháy trong không khí cho ngọn lửa xanh mờ. Đưa lưu huỳnh đang cháy vào bình đựng khí oxi, lưu huỳnh tiếp tục cháy cho ngọn lửa
A.
sáng hơn và sinh ra lưu huỳnh đioxit.B.mờ hơn và sinh ra lưu huỳnh đioxit.C.sáng hơn và sinh ra lưu huỳnh trioxit.D.mờ hơn và sinh ra lưu huỳnh trioxit.
Câu 2:Trộn sắt bột và lưu huỳnh bột rồi cho vào ống nghiệm khô. Đun ống nghiệm trên ngọn lửa đèn cồn, một lúc sau hỗn hợp cháy đỏ. Sản phẩm tạo thành là
A.
sắt(II) sunfua có màu nâu đỏ.B.sắt(II) sunfua có màu xám đen.C.sắt(III) sunfua có màu nâu đỏ.D.sắt(III) sunfua có màu xám đen.
A.
điện phân nước.B.nhiệt phân Cu(NO3)2C.nhiệt phân KClO3có xúc tác MnO2.D.chưng cất phân đoạn không khí lỏng.
Câu 4-10:Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mụcHỏi đápđể cùng cộng đồng Hóa pgdngochoi.edu.vn thảo luận và trả lời nhé.

Hoá học 10 Bài 29: Oxi - Ozon
Hoá học 10 Bài 30 Lưu huỳnh
Hoá học 10 Bài 32 Hiđro sunfua - Lưu huỳnh đioxit - Lưu huỳnh trioxit
Toán 10
Lý thuyết Toán 10









